Espectroscopia de Fluorescencia parte II / Experimento con el espectrómetro de rejilla- espectroscopia de emisión
Saludos amigos amantes de la ciencia. En el post anteriorhable sobre la espectroscopia de fluorescencia y mencione que mostraría un experimento básico con el uso del espectrómetro de rejilla, a continuación explicare detalladamente en qué consiste este experimento.
Como he venido escribiendo durante los últimos meses, sabemos que la espectroscopia es aquella que se encarga del estudio de la materia a través de la radiación electromagnética. En este post nos centraremos en la espectroscopia de emisión, a través de esta procederemos a identificar tres tipos de gases distintos desconocidos a primera instancia, todo esto de acuerdo a la observación de las líneas espectrales que se identifican a través del espectrómetro. Antes de eso debemos conocer cómo está compuesto este equipo, su calibración y detalles importantes acerca de la composición para una medida confiable.
> La espectrometría de emisión es una técnica que sirve para analizar longitudes de onda de los fotones emitidos por los átomos o moléculas durante su transición desde un estado excitado a un estado de inferior energía. Cada elemento emite un conjunto característico de longitudes de onda discretas en función de su estructura electrónica. Mediante la observación de estas longitudes de onda puede determinarse composición elemental de la muestra.
Podemos identificar y separar con una rejilla de difracción diferentes líneas espectrales. Los diferentes haces de luz envueltos en este fenómeno con su respectiva longitud de onda deben superponerse y así producir líneas muy nítidas de diversos colores según dependiendo el material que se está identificando, en la rejilla la luz sufre una difracción y es difractada de una onda larga a una onda corta.
Un espectrómetro básico tiene 3 componentes esenciales para su funcionamiento estos son:
Colimador: Está formado por una pequeña rejilla cuya función es hacer más pequeña la luz y poder direccionar correctamente hacia el componente que difracta dicha luz.
Este Componente difractante se encarga de doblar el haz de luz y luego este se divida formando un espectro de luz visible, a su vez está conformado internamente por un prisma que es el que dispersa esta luz.
Cabe destacar que al contar las desviaciones de cada línea del espectro de un gas o cualquier elemento que nosotros queremos identificar, podemos calcular las longitudes de onda correspondiente a este espectro. En base a ellas puede luego determinarse, por comparación con valores de tabla adecuados, la fuente de luz.
Ocular: por medio de este son observadas las líneas espectrales resultantes de la difracción del haz para medir la longitud de onda de cada una.
Para la práctica con el espectrómetro de rejilla debemos tomar en cuenta ciertas consideraciones para realizar unas medidas de forma correcta, en esta oportunidad voy a explicar resumidamente tips esenciales para un ajuste adecuado
del espectrómetro.
Realizar medidas precisas y confiables significa que debemos tener un espectrómetro perfectamente calibrado, este equipo se debe ajustar con cuidado ya que gran parte de sus piezas son muy delicadas. La rendija y retícula son 2 componente que debe estar direccionadas en el plano focal, es decir en la vía donde pasa el haz de luz y se difracta hacia el telescopio, estas a su vez deben estar paralelas al eje de rotación del telescopio. Para poder observar las líneas espectrales de forma correcta y que se puedan diferenciar, el medio ambiente se recomienda estar en total oscuridad esto facilita también el ajuste del espectrómetro.
Importante: durante el ajuste previo del equipo, la mesa juega un papel fundamental en el momento de su calibración, la inclinación de esta puede variar dentro de ciertos parámetros. Lo ideal es que la mesa del prisma este en una posición horizontal para poder controlar su calibración a simple vista.
Hay que decir que ciertas personas que sufren de alguna enfermedad ocular pueden observar los objetos lejanos con el telescopio, este no necesariamente se debe enfocar hacia el infinito como dicen algunas personas, ¡esto es totalmente falso! Sin embargo, se pueden realizar mediciones eficaces si por la persona ajusta de forma correcta el colimador con el telescopio enfocado hacia el infinito. Se puede deslizar el ocular con la finalidad de lograr mayor nitidez y así las personas puedan observar fácilmente las líneas espectrales. Puesto que la imagen del material debe encontrarse con el plano focalizado, no debe existir paralelaje entre el objeto y el retículo, debe estar correctamente enfocado.
El montaje del experimento es bastante simple, en primer lugar, debemos fijar la lámpara espectral de He junto con la base del soporte, debemos conectar la bobina que genera la corriente y posteriormente encenderla. La lámpara de He debe iluminar completamente la rendija, hacer énfasis en encontrar el eje óptico adecuado de las lámparas al colimador. Debemos posicionar la rejilla sobre la mesa del prisma para que al momento de realizar las mediciones colocar el telescopio de forma que el haz de luz pueda atravesar la rendija y así iluminar por completo la rejilla, de esta forma podemos observar los espectros cómodamente a través del ocular.
Si deseamos realizar mediciones precisas es importante ubicar la rejilla sobre el eje de rotación del telescopio y a su vez direccionar verticalmente al eje óptico del colimador, es decir la mitad de la mesa del prisma.
La resolución tiende a crecer a medida que decrece el ancho de la rendija, a su vez que la intensidad lumínica del espectro se hace menor. Y finalmente con el tornillo micrométrico llevar el ancho de la rendija a un valor adecuado.
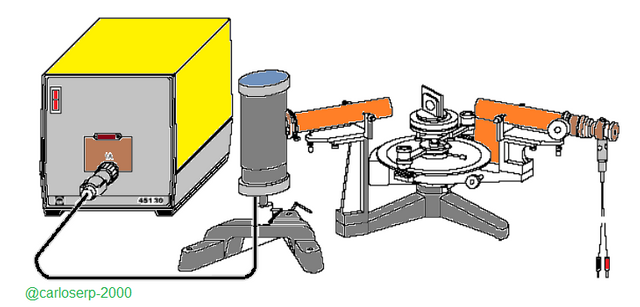
Montaje experimental de espectrómetro de rejilla donde se se pueden observar sus diferentes componentes, como fuente, telescopio, mesa de prisma, lupas, oculares, disco graduado, colimador.
Ahora bien, luego de haber explicado lo anterior procederemos a identificar 3 tipos de gases diferentes. Para este procedimiento como se ha desarrollado en los puntos anteriores se necesita una resistencia variable entre la fuente y uno de los electrodos sobre el cual debe estar fijado el tubo contenedor del gas a identificar, en este caso el mercurio, el tubo está ubicado en frente del colimador. Otra forma de calibrar el espectrómetro es usar un tubo contenedor con un gas ya conocido, en este caso utilizamos el mercurio ya que sus líneas espectrales son muy fáciles de observar y conocemos sus longitudes de onda correspondientes, esto se hace para poder ajustar adecuadamente la escala del espectrómetro.
Una vez calibrado el equipo pasamos a la siguiente etapa que es identificar los 3 tipos de gases y sus respectivas longitudes de onda, finalmente se realizará una comparación con estudios teóricos y así finalmente poder identificar qué tipo de gas estamos observando.
Para calcular las longitudes de onda debemos usar una ecuación muy famosa, donde uno de los científicos destacados fue Johann Balmer, el cual ideó un modelo matemático mediante el cual podían ser obtenidas las longitudes de onda características de las líneas espectrales del hidrógeno y elementos similares. Más tarde Johannes Rydberg mejoría este modelo haciéndolo en dependencia del número de onda en vez d su longitud, a esto fue agregado un valor constante el cual lleva su nombre como:
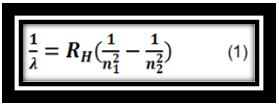
Donde λ es la longitud de onda, RH es la constante de Rydberg, n1 y n2 son los valores que representan los niveles orbitales del átomo, los cuales determinan la serie a utilizar, para el presente estudio fue de utilidad la llamada serie de Balmer.

Vamos a realizar el experimento.
Como mencione utilizaremos el mercurio como elemento de calibración del espectrómetro, en la siguiente tabla se muestran las respectivas longitudes de onda correspondientes al gas de mercurio.
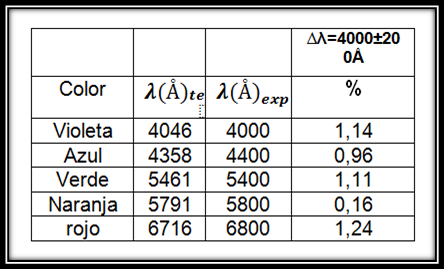
Longitudes de onda del espectro de emisión del mercurio
Luego de calibrar el equipo y visualizar cada línea espectral del gas de mercurio, procedemos a identificar los 3 tubos contenedores de gases desconocidos y luego de haber identificado cada línea espectral correspondiente a cada gas, debemos comparar los valores experimentales con los valores teóricos basándose en un programa especializado para identificar espectro de gases llamado Atomic Spectra.
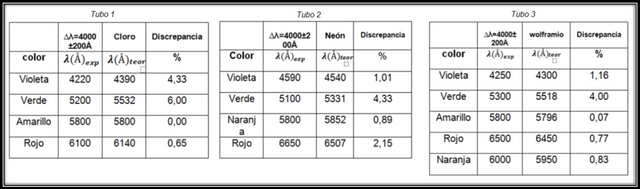
Luego de hacer las comparaciones experimentales de espectro de emisión con los datos teóricos se han identificado cada tubo de acuerdo a color de cada línea espectral, el primer tubo pertenece a las líneas espectrales del Cloro. El segundo tubo pertenece al Neón y finalmente el tercer tubo pertenece al espectro del Wolframio.
La parte final del experimento consiste en calcular la constante Rydberg del tubo de mercurio, con los resultados obtenidos experimentalmente de cada espectro, esta constante tiene un valor teórico de 1,097x107 m-1 , el cual compararemos y obtendremos su discrepancia %.
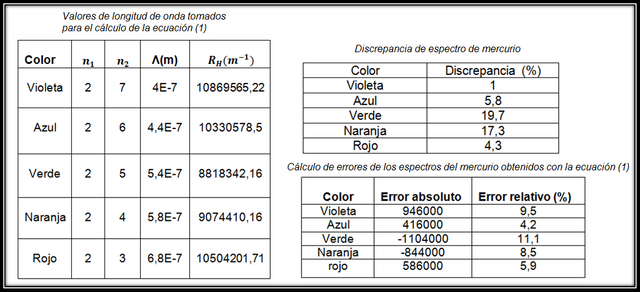
Para concluir la espectroscopia es un campo muy amplio, como he venido compartiendo los últimos meses tiene gran variedad de técnicas y podría decirse que es usada en todos los campos de la ciencia. Este experimento sobre el espectrómetro de rejilla basado en la espectroscopia de emisión y fluorescencia es un tema que se dicta en la carrera de licenciatura en física, un tema básico e importantes para los estudiantes de la carrera. En este experimento los objetivos se cumplieron de forma exitosa ya que pudimos visualizar a través del aparato líneas espectrales de diferentes gases y así mismo identificar qué tipo de gas correspondía cada tubo y de igual forma calcular las longitudes de onda correspondientes, como la constante de Rydberg, con un margen de error o discrepancia del 0,92 para el mercurio, 2,7 para el cloro, 2,1 para el neón y 1,37 para el wolframio.
Importante recordar que para realizar este experimento se deben tomar ciertas consideraciones como por ejemplo una buena calibración y ajuste de cada componente del equipo para así poder obtener resultados viables.
Para más información
Robert Eisberg y Robert Resnick. “FISICA CUANTICA”. 2011. Editorial Limusa Wiley. P 126-130.
Mark Kness, 2002. Aplicación AtomicSpectra V1.0 Copyright 2002.
MEDICION DE LINEAS ESPECTRALES
Espectroscopía: la interacción de la luz y la materia
Únete al trail de STEM-Espanol

No olvides votar por @stem.witness como testigo

Ahora puedes escribir tus publicaciones a través de la app oficial https://www.steemstem.io y obtendrás un voto extra del 5%

This post has been voted on by the SteemSTEM curation team and voting trail in collaboration with @utopian-io.
If you appreciate the work we are doing then consider voting both projects for witness by selecting stem.witness and utopian-io!
For additional information please join us on the SteemSTEM discord and to get to know the rest of the community!
To listen to the audio version of this article click on the play image.

Brought to you by @tts. If you find it useful please consider upvoting this reply.
¡Felicitaciones!
Te participamos que puedes invertir en el PROYECTO ENTROPÍA mediante tu delegación de Steem Power y así comenzar a recibir ganancias de forma semanal transferidas automáticamente a tu monedero todos los lunes. Entra aquí para más información sobre cómo invertir en ENTROPÍA.
Apoya al trail de @Entropia y así podrás ganar recompensas de curación de forma automática. Entra aquí para más información sobre nuestro trail.
Puedes consultar el reporte diario de curación visitando @entropia.
Atentamente
El equipo de curación del PROYECTO ENTROPÍA
Saludos mi estimado @carloserp-2000, que interesante leer cada una de tus publicaciones de espectroscopia y conocer el gran campo que este abarca y la importancia de una buena calibración para poder tener resultados exactos.
Congratulations @carloserp-2000! You have completed the following achievement on the Steem blockchain and have been rewarded with new badge(s) :
Click here to view your Board
If you no longer want to receive notifications, reply to this comment with the word
STOPTo support your work, I also upvoted your post!
@carloserp-2000 You have received a 100% upvote from @intro.bot because this post did not use any bidbots and you have not used bidbots in the last 30 days!
Upvoting this comment will help keep this service running.
Saludos @carloserp-2000. Excelente trabajo sobre la espectroscopia de emisión. Sin duda un tema que no puede faltar en nuestra formación. Muy clara y didáctica tu presentación. Gracias por compartirlo.
Muchas gracias profesor este experimento que nunca es olvidado con el transcurrir de los años :)
Hi @carloserp-2000!
Your post was upvoted by Utopian.io in cooperation with @steemstem - supporting knowledge, innovation and technological advancement on the Steem Blockchain.
Contribute to Open Source with utopian.io
Learn how to contribute on our website and join the new open source economy.
Want to chat? Join the Utopian Community on Discord https://discord.gg/h52nFrV